近日浩广配资,百时美施贵宝(BMS)公布了Cobenfy (KarXT)作为成人精神分裂症辅助治疗的III期临床试验ARISE顶线结果,试验结果显示,与对照组相比,KarXT组在PANSS量表评分上未达到显著差异,错过主要终点目标。
主要次要终点都没达到
ARISE是一项为期6周的双盲、多中心、安慰剂对照的Ⅲ期临床试验,主要在成年精神分裂症患者中评估了KarXT作为非典型抗精神病药物辅助方案的安全性和有效性。
试验结果显示,与对照组(安慰剂+非典型抗精神病药物)相比,接受“KarXT+非典型抗精神病药物”治疗的患者在第6周时PANSS量表评分改善了2.1分(-14.3分 VS -12.2分),两者之间未能达到显著性差异。此外,在PSP量表和CGI-S量表等次要终点上,KarXT组与安慰剂组之间没达到统计学上的显著差异。
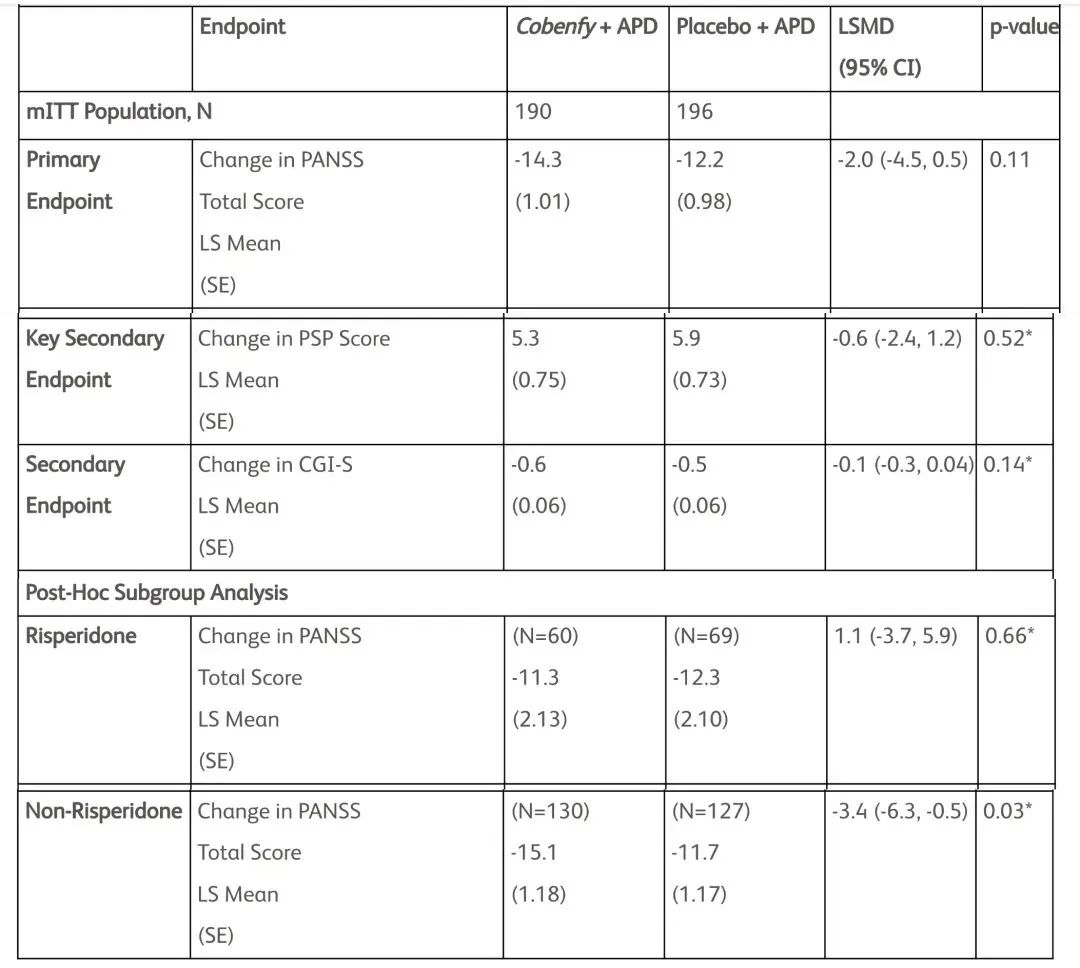
值得一提的是,在非利培酮亚组中,KarXT组与对照组相比之间的PANSS评分显示出显著差异(-15.1 VS -11.7)。
安全性方面,KarXT联合用药的安全性与耐受性与其单药治疗一致。
基于该临床结果,BMS表示将进行进一步的数据分析,并与监管机构讨论下一步行动。目前BMS正在针对推进KarXT在阿尔茨海默病、自闭症谱系障碍、双相情感障碍等多种神经/精神疾病的临床开发。
一个季度卖了1000万美元浩广配资
KarXT为BMS巨资140亿美元收购Karuna Therapeutics公司而来,是数十年来首个获批治疗精神分裂症的新机制药物。2024年9月获得FDA批准用于治疗精神分裂症成人患者。
一直以来,精神病的新药开发是出了名的困难,严重的副作用是长期以来困扰精神病药物开发的棘手难题。
FDA批准KarXT最主要原因就是最大安全性,在其临床中出现的常见不良事件主要是轻中度胃肠道副作用。
在此之前,常用被批准用于精神病药物主要通过抑制D2多巴胺受体起作用,不仅疗效一般且带有严重的副作用问题,据统计,至少有一半患者根本无法坚持治疗。
而KarXT通过针对完全不同的神经递质系统——毒蕈碱乙酰胆碱型受体(M受体)来减少严重副作用,KarXT既包含了M受体的激活剂Xanomeline,又包含了M受体的拮抗剂Trospium。KarXT通过将Xanomeline和Trospiu组合,旨在优先刺激中枢神经系统的M受体,而同时避免刺激周围神经组织M受体,减少副作用,同时改善精神病症状。

上市之后,KarXT的销售表现不错,20224年Q4单季度便卖了1000万美元,另外,再鼎医药还引进了KarXT大中华区(包括中国内地、中国香港、中国澳门和中国台湾地区)独家权益。去年年底,再鼎已在中国提交了KarXT新药上市申请。
本周好文推荐如需转载请联系佰傲谷并在醒目位置注明出处
]article_adlist-->

 ]article_adlist-->
]article_adlist--> ]article_adlist-->
]article_adlist-->
 海量资讯、精准解读,尽在新浪财经APP
海量资讯、精准解读,尽在新浪财经APP
互盈策略提示:文章来自网络,不代表本站观点。